消息,2024年5月10日百济神州(688235)发布公告称公司于2024年5月9日接受机构调研,3W Fund、Manulife、Ocean link Management、Orbimed、PICC、Prudence Investment、Schroders、Taiping AM HK、Temasek、UBS、Zeal Asset Management、Ariose Capital、安信基金、贝莱德基金、彼得明奇资管、财通证券、查理投资、成吉思汗基金、崇山投资、淳厚基金、大成国际、德同资本、Bocom International、东财医药、东方阿尔法基金、东海证券、东吴基金、东吴医药、东证资管、服贸基金、复星财富、高毅资产、光证资管、Boyu Capital、广发证券、广州高新科控、国都资管、国君资管、国寿资产、国泰君安证券、国新证券、国信证券、海通国际、海通资管、China Innovation Capital、和谐汇一、红杉资本、湖南医药发展私募基金管理有限公司、华宝基金、华福证券、华泰资产、华西证券、华夏基金(香港)有限公司、汇丰晋信、汇添富基金、Exome、惠理基金、惠升基金、混沌投资、嘉富投资、嘉实基金、建信养老、交银施罗德、聚润资本、君和资本、名禹资产、Franklin Templeton Investments、鹏华基金、平安养老基金、睿远基金、山东铁路发展基金、陕西金控、上海博润投资管理有限公司、上海峰境基金、上海贵源投资有限公司、上银基金、申万宏源、J.P. Morgan Asset Management、泰康资产、天风证券、新丝路基金、兴业证券、兴证国际资管、阳光保险资产、野村东方国际证券、英大基金、圆信永丰基金、招商局集团、Manhattan Capital、招商信诺、招商银行股份有限公司昆明分行、招银国际、招证国际、中金公司、中信资管、中邮基金、中再资产、重阳投资、朱雀基金参与。
具体内容如下:
问:请管理层介绍一季度公司财务情况?
答:2024年第一季度,总收入达53.59元,较上年同比上升74.8%,主要得益于百悦泽?在美国和欧洲的销售额分别同比增长162.7%和256.8%。产品收入为53.25,上年同期产品收入为28.08亿元。产品收入增加的原因是公司自研产品百悦泽?和百泽安?的销售额增加。截至2024年3月31日止三个月内,美国是公司最大的市场,产品收入达24.96亿元,同比增长162.7%。2024年第一季度毛利占全球产品收入的83%;相比较,去年同期为80%。毛利率增长主要是由于与产品组合中的其他产品相比,百悦泽?在全球销售中占比更高。2024年第一季度,公司在美国一般公认会计准则下的经营亏损同比下降30%,经调整经营亏损同比下降47%。公司继续保持收入大幅增长和费用控制,在迈向可持续盈利的道路上取得进一步进展。截至2024年3月31日,公司的现金和现金等价物为28亿美元。
问:请管理层介绍一季度BTK全球销售继续保持优势的原因?BTK在全球的销售放量和患者覆盖如何?
答:2024年第一季度,百悦泽?全球销售额总计34.76亿元,同比增长140.2%,在血液肿瘤领域进一步巩固领导地位。其中,美国销售额总计24.96亿元,同比增长162.7%,主要得益于该产品在初治(TN)慢性淋巴细胞白血病(CLL)中的市场份额有所提升,同时在复发或难治性(R/R)CLL新增患者中的市场份额也已领先于同类BTK抑制剂药物。欧洲销售额总计4.76亿元,同比增长256.8%,主要得益于市场份额的不断扩大,以及在多地纳入医保,包括法国首次对百悦泽?的CLL、华氏巨球蛋白血症(WM)和边缘区淋巴瘤(MZL)适应症进行报销。百悦泽?获得美国FD、欧盟委员会和加拿大卫生部批准,用于治疗既往接受过至少两线系统性治疗的R/R滤泡性淋巴瘤(FL)成人患者,成为迄今为止首个在该项适应症获批的BTK抑制剂,也是美国和欧盟地区适用患者人群最广泛的BTK抑制剂。中国销售额总计4.13亿元,同比增长25.5%,主要得益于该产品在已获批适应症领域的销售额增长。公司在中国BTK抑制剂市场的市场份额持续保持领导地位。目前,百悦泽?在中国获批的5项适应症已全部纳入国家医保目录。
问:请管理层介绍百泽安?在海外的商业化进展?
答:百泽安?于2023年9月获得欧盟委员会批准,作为单药用于治疗既往接受过含铂化疗的不可切除、局部晚期或转移性食管鳞状细胞癌(ESCC)的成人患者。百泽安?已在美国和英国取得批准用于二线治疗食管鳞状细胞癌(ESCC)成人患者,并在欧盟获批联合化疗用于一线和单药用于二线治疗转移性非小细胞肺癌(NSCLC)的三项适应症。公司已建立了具有差异化的全球商业化团队,规模超过3,700人,其中500多人分布于北美和欧洲。百悦泽?在全球范围内的商业化成功已验证了公司商业化团队的实力,百泽安?的海外市场准入及销售团队组建工作正在顺利推进中。
问:请介绍艾伯维专利诉讼进展?
答:美国专利商标局(USPTO)批准了公司的申请,将对Pharmacyclics在专利侵权诉讼中指控公司所侵犯的专利进行授权后复审,并表示公司已证明该专利无效的可能性大于百分之五十。预计USPTO将在12个月内就该专利的有效性作出最终裁决。公司对百悦泽?的知识产权有充分的信心,并将继续研发更有效、更安全的创新型肿瘤治疗方案。公司也将一如既往地致力于为全世界癌症患者提供更多可及、可负担的药物。
问:请介绍公司BCL2抑制剂sonrotoclax(BGB-11417)的最新进展?
答:BCL2抑制剂sonrotoclax(BGB-11417)作为单药治疗以及与核心药物百悦泽?的联合疗法正在开发中。公司正在继续推进sonrotoclax的四项注册性临床试验,包括sonrotoclax联合百悦泽?用于一线治疗CLL患者的一项全球关键性三期试验、用于R/R华氏巨球蛋白血症(WM)和R/R套细胞淋巴瘤(MCL)的两项潜在全球注册可用二期临床试验,以及用于R/R CLL的一项潜在中国注册可用二期临床试验,目前已入组受试者超过850人。其中,R/R MCL适应症已获得美国FD快速通道资格认定。
问:请介绍BTK CDAC (BGB-16673)的进展?
答:公司已启动靶向BTK的嵌合式降解激活化合物(CDC)BGB-16673的关键研究项目。BTK CDC用于治疗R/R MCL(潜在注册可用)和R/R CLL的两项扩展队列研究目前已入组受试者超过220人,并预计将于2024年底前启动R/R CLL的三期临床试验。
问:请介绍公司在实体瘤研发主要管线方面的进展?
答:肺癌领域(1)欧司珀利单抗(抗TIGIT抗体)用于PD-L1高表达NSCLC一线治疗的3期临床试验完成末例受试者入组。(2)替雷利珠单抗与BGB-45(抗OX40抗体)、LBL-007(抗LG-3抗体)和BGB-15025(HPK1抑制剂)联用治疗肺癌的多个队列,预计将于2024年内进行数据读出。(3)泛KRS抑制剂、MT协同PRMT5抑制剂,以及EGFR CDC有望在2024年下半年进入临床。乳腺癌领域(1)BGB-43395(CDK4抑制剂)启动单药治疗的第四个剂量水平给药,该剂量处于有效剂量范围内,未观察到剂量限制性毒性;首个单药治疗剂量开始给药后,仅4个多月即启动与氟维司群的联合用药。(2)BG-68501(CDK2抑制剂)在首次人体临床试验中启动单药治疗的第二个剂量水平给药,临床药代动力学符合预期,未观察到剂量限制性毒性。(3)BG-C9074(B7H4 DC)在全球首次人体临床试验1期研究中,在澳大利亚完成首例患者给药。胃肠癌领域(1)2024年,替雷利珠单抗与LBL-007(抗LG-3抗体)和BGB-45(抗OX40抗体)联合用药的多个队列将进行数据读出。(2)计划向中国国家药品监督管理局(NMP)提交泽尼达妥单抗用于二线治疗胆道癌的新药上市许可申请。(3)CE-DC和FGFR2b-DC有望在2024年下半年进入临床。
问:请管理层介绍投资者关注的未来盈利计划?
答:本季度公司再次展现出强劲的财务业绩表现。得益于全球收入的大幅增长,按抗肿瘤药物总销售额计算,公司现已跻身全球肿瘤治疗创新公司前15强。此外,在实现可持续盈利的过程中,公司的经营效率也在继续大幅提升。公司已经完成了全方位一体化的全球肿瘤治疗创新公司的基础设施建设,拥有涵盖早期药物发现、临床前研究、全球临床试验运营、自主规模化药物生产与商业化等创新药开发全周期的能力。公司预计在2024年产品收入将继续增长,并且产品收入的增幅将超过经营费用的增幅,使公司能够持续保持经营优势。公司将继续谨慎且战略性地部署资金,并致力于创造长期价值,提高股东报。
百济神州(688235)主营业务:研究、开发、生产以及商业化创新型药物。
百济神州2023年年报显示,公司主营收入174.23亿元,同比上升82.13%;归母净利润-67.16亿元,同比上升50.77%;扣非净利润-96.82亿元,同比上升29.97%;其中2023年第四季度,公司单季度主营收入45.48亿元,同比上升68.6%;单季度归母净利润-28.38亿元,同比上升11.55%;单季度扣非净利润-28.99亿元,同比上升11.52%;负债率38.95%,投资收益1.67亿元,财务费用1.97亿元,毛利率84.57%。
该股最近90天内共有8家机构给出评级,买入评级7家,增持评级1家;过去90天内机构目标均价为186.19。
以下是详细的盈利预测信息:
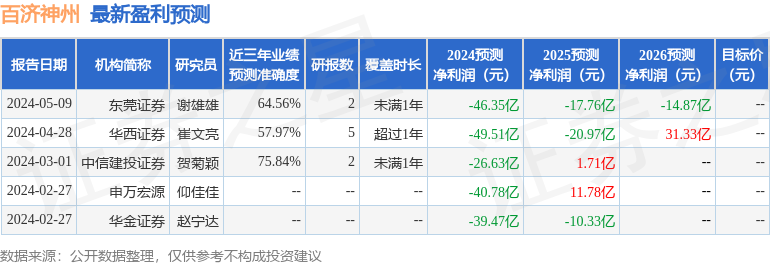
融资融券数据显示该股近3个月融资净流出1.27亿,融资余额减少;融券净流出454.72万,融券余额减少。
以上内容由根据公开信息整理,由算法生成(网信算备310104345710301240019号),与本站立场无关,如数据存在问题请联系我们。本文为数据整理,不对您构成任何投资建议,投资有风险,请谨慎决策。